코로나19와 바이오제약업계
코로나19와 바이오제약업계

코로나19 백신 개발, 어디까지 왔을까?
코로나19 백신개발,
어디까지 왔을까?
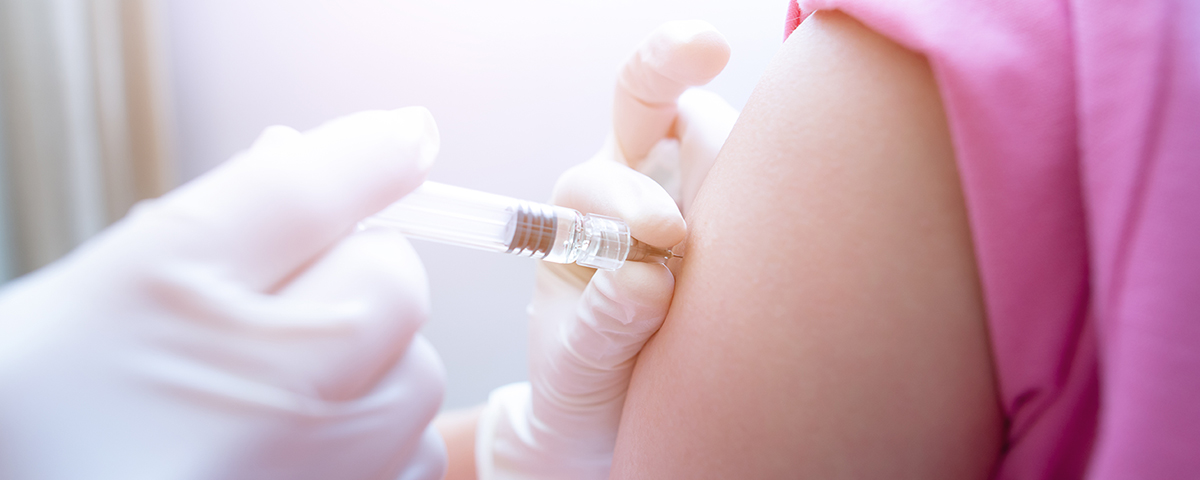
하지만 백신을 단기간에 개발하기란 결코 쉽지 않습니다. 일반적으로 백신 개발은 후보물질을 탐색하고 찾아낸 뒤, 동물을 대상으로 한 전임상 시험과 인체를 대상으로 한 3단계의 임상시험을 통해 효능과 안전성을 확인한 후 최종 승인을 받는 방식으로 이루어집니다. 이 과정에서 평균 5~10년의 오랜 기간이 걸리며 막대한 비용 또한 소요되죠. 그러나 실험 중인 백신이 최종 승인을 받는 확률은 단 6%에 불과합니다.2 효능과 안전성, 엄격한 품질 관리, 대량 생산 가능 여부와 같은 까다로운 조건을 모두 충족하는 단 하나의 후보만이 이 모든 과정을 거쳐 백신으로 탄생할 수 있습니다.
하지만 백신을 단기간에 개발하기란 결코 쉽지 않습니다. 일반적으로 백신 개발은 후보물질을 탐색하고 찾아낸 뒤, 동물을 대상으로 한 전임상 시험과 인체를 대상으로 한 3단계의 임상시험을 통해 효능과 안전성을 확인한 후 최종 승인을 받는 방식으로 이루어집니다. 이 과정에서 평균 5~10년의 오랜 기간이 걸리며 막대한 비용 또한 소요되죠. 그러나 실험 중인 백신이 최종 승인을 받는 확률은 단 6%에 불과합니다.2 효능과 안전성, 엄격한 품질 관리, 대량 생산 가능 여부와 같은 까다로운 조건을 모두 충족하는 단 하나의 후보만이 이 모든 과정을 거쳐 백신으로 탄생할 수 있습니다.
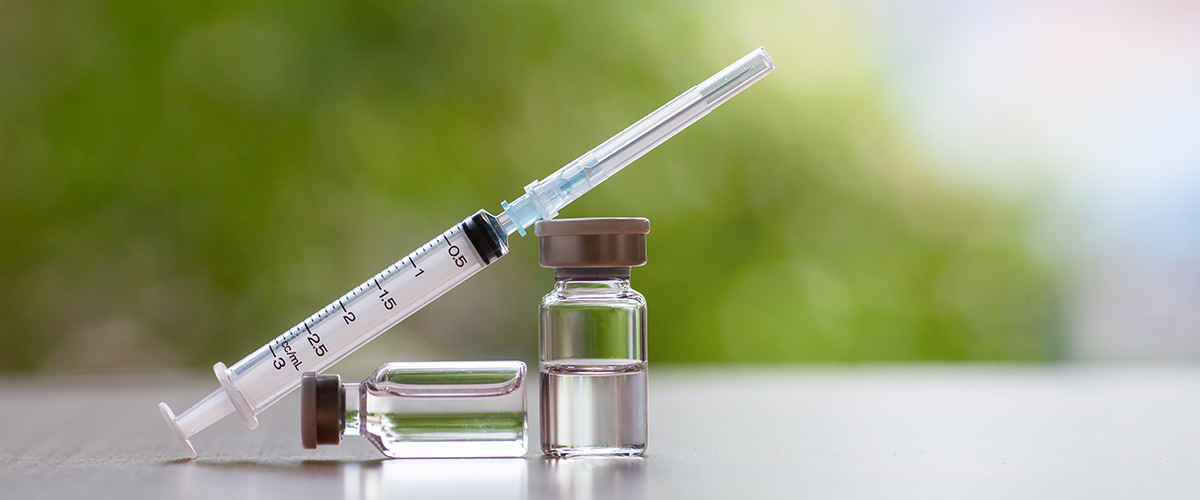

1단계 : 바이러스와 유전자 배열 분석
2020년 1월 10일, 중국 보건 당국자들은 첫 번째 사례가 발견된 지 불과 몇 주 만에 신종 코로나바이러스의 전장 유전체를 분석한 논문을 발표했고, 다음 날 전 세계의 연구자들은 백신 연구에 돌입했습니다. 2002년 사스 발견 당시 전장 SARS-CoV-1 유전자 코드를 배열하는 데 수 개월이 걸린 것과 비교하면, 최신 기술의 발전으로 코로나19 바이러스를 분류하고 잠재적인 백신을 만드는 데 걸리는 시간이 획기적으로 단축됐습니다.

1단계 : 바이러스와 유전자 배열 분석
2020년 1월 10일, 중국 보건 당국자들은 첫 번째 사례가 발견된 지 불과 몇 주 만에 신종 코로나바이러스의 전장 유전체를 분석한 논문을 발표했고, 다음 날 전 세계의 연구자들은 백신 연구에 돌입했습니다. 2002년 사스 발견 당시 전장 SARS-CoV-1 유전자 코드를 배열하는 데 수 개월이 걸린 것과 비교하면, 최신 기술의 발전으로 코로나19 바이러스를 분류하고 잠재적인 백신을 만드는 데 걸리는 시간이 획기적으로 단축됐습니다.

2단계 : 백신의 종류 결정
신종 코로나바이러스에 대응하기 위한 안전하고 효과적인 백신이 절실히 필요한 상황에서, 전 세계의 바이오의약품 연구자들은 하나 또는 그 이상의 접근법에 대한 성공 확률을 높이기 위해 광범위한 접근법들을 시험하고 있습니다.

2단계 : 백신의 종류 결정
신종 코로나바이러스에 대응하기 위한 안전하고 효과적인 백신이 절실히 필요한 상황에서, 전 세계의 바이오의약품 연구자들은 하나 또는 그 이상의 접근법에 대한 성공 확률을 높이기 위해 광범위한 접근법들을 시험하고 있습니다.
3단계 : 전임상 시험 시행
주목할 만한 사실은 이 단계에서 흔히 많은 백신 후보들이 실패하기 때문에 가능한 많은 후보가 필요하다는 것입니다.

3단계 : 전임상 시험 시행
주목할 만한 사실은 이 단계에서 흔히 많은 백신 후보들이 실패하기 때문에 가능한 많은 후보가 필요하다는 것입니다.

4단계 : 임상 시험 시행
전임상 시험 단계에서 성공한 잠재적 백신은 인체를 대상으로 한 여러 단계의 임상 시험에 돌입하게 됩니다. 초기 단계의 시험은 수십 명의 참가자를 대상으로 새로운 백신의 안전성과 최적화된 투여 량을 시험합니다. 대부분의 주요 임상 시험과 달리 백신에 대한 임상 시험이 갖는 독특한 점은 건강한 참가자를 대상으로 한다는 사실입니다. 따라서 백신의 효능을 증명하기 위해서는 다른 치료제보다 더 긴 기간과 더 큰 규모의 임상 시험을 필요로 할 수 있습니다.
추가적인 시험에서는 수백 또는 수천 명의 참가자를 대상으로 백신에 대해 면역체계가 어떻게 반응하는지, 백신이 효과적이고 내구성이 있는지 여부와 함께 백신의 안전성 프로파일을 더 잘 이해하기 위한 검사를 진행합니다. 백신의 안전성을 보다 잘 이해하기 위해 연구 중인 백신과 질병의 종류에 따라 수천 또는 수만 명의 참가자가 참여할 수도 있습니다. 2020년 5월 1일 기준 초기 임상실험에 진입한 백신 후보들은 9개에 불과하였으나, 2022년 10월 28일 기준으로 172개 백신 후보들에 대한 임상시험이 진행 중에 있습니다.

4단계 : 임상 시험 시행
전임상 시험 단계에서 성공한 잠재적 백신은 인체를 대상으로 한 여러 단계의 임상 시험에 돌입하게 됩니다. 초기 단계의 시험은 수십 명의 참가자를 대상으로 새로운 백신의 안전성과 최적화된 투여 량을 시험합니다. 대부분의 주요 임상 시험과 달리 백신에 대한 임상 시험이 갖는 독특한 점은 건강한 참가자를 대상으로 한다는 사실입니다. 따라서 백신의 효능을 증명하기 위해서는 다른 치료제보다 더 긴 기간과 더 큰 규모의 임상 시험을 필요로 할 수 있습니다.
추가적인 시험에서는 수백 또는 수천 명의 참가자를 대상으로 백신에 대해 면역체계가 어떻게 반응하는지, 백신이 효과적이고 내구성이 있는지 여부와 함께 백신의 안전성 프로파일을 더 잘 이해하기 위한 검사를 진행합니다. 백신의 안전성을 보다 잘 이해하기 위해 연구 중인 백신과 질병의 종류에 따라 수천 또는 수만 명의 참가자가 참여할 수도 있습니다. 2020년 5월 1일 기준 초기 임상실험에 진입한 백신 후보들은 9개에 불과하였으나, 2022년 10월 28일 기준으로 172개 백신 후보들에 대한 임상시험이 진행 중에 있습니다.

5단계 : 시판 승인 획득

5단계 : 시판 승인 획득
6단계 : 생산 및 유통
전 세계, 특히 저개발 지역의 환자들에게 백신을 안전하게 제공하는 것도 어려운 과제 중 하나입니다. 백신은 유통과정에서 온도 조절과 같은 특수 처리가 필요한 경우가 많기 때문입니다. 바이오제약업계에서는 현지 정부 및 NGO 파트너들과의 긴밀한 협력을 통해 전 세계로 백신을 보급할 수 있는 가능성에 대비한 기초 작업을 진행하고 있습니다.
6단계 : 생산 및 유통
전 세계, 특히 저개발 지역의 환자들에게 백신을 안전하게 제공하는 것도 어려운 과제 중 하나입니다. 백신은 유통과정에서 온도 조절과 같은 특수 처리가 필요한 경우가 많기 때문입니다. 바이오제약업계에서는 현지 정부 및 NGO 파트너들과의 긴밀한 협력을 통해 전 세계로 백신을 보급할 수 있는 가능성에 대비한 기초 작업을 진행하고 있습니다.




